Physikalisch-chemische Eigenschaften von Alkylpolyglycosiden – Phasenverhalten
Binäre Systeme
Das Phasendiagramm des C12-14-Alkylpolyglycosids (C12-14 APG)/Wasser-Systems unterscheidet sich von dem des kurzkettigen APG (Abbildung 3). Bei niedrigeren Temperaturen bildet sich über einen weiten Konzentrationsbereich ein Fest-/Flüssigbereich unterhalb des Krafft-Punkts. Bei steigender Temperatur geht das System in eine isotrope Flüssigphase über. Da die Kristallisation kinetisch stark verzögert ist, ändert diese Phasengrenze ihre Position mit der Lagerzeit. Bei niedrigen Konzentrationen geht die isotrope Flüssigphase oberhalb von 35 °C in einen Zweiphasenbereich mit zwei flüssigen Phasen über, wie dies normalerweise bei nichtionischen Tensiden beobachtet wird. Bei Konzentrationen über 60 Gew.-% bildet sich bei allen Temperaturen eine Abfolge flüssigkristalliner Phasen. Erwähnenswert ist, dass im isotropen Einphasenbereich eine deutliche Strömungsdoppelbrechung zu beobachten ist, wenn die Konzentration knapp unter der der gelösten Phase liegt, und diese dann nach Abschluss des Scherprozesses schnell verschwindet. Es wurde jedoch kein von der L1-Phase getrennter Mehrphasenbereich gefunden. In der L1-Phase befindet sich ein weiterer Bereich mit schwacher Strömungsdoppelbrechung in der Nähe des Minimalwerts der Flüssig/Flüssig-Mischungslücke.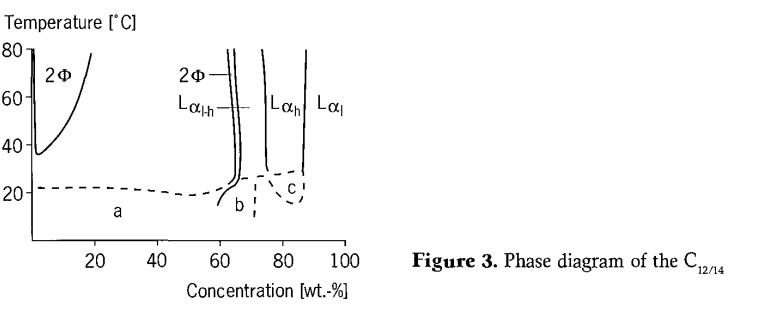
Phänomenologische Untersuchungen zur Struktur der flüssigkristallinen Phasen wurden von Platz et al. durchgeführt. Dabei kamen Methoden wie die Polarisationsmikroskopie zum Einsatz. Nach diesen Untersuchungen werden drei verschiedene lamellare Regionen in konzentrierten C12-14 APG-Lösungen betrachtet: Lαich ,Lαlinksund Lαh. Laut Polarisationsmikroskopie gibt es drei verschiedene Texturen.
Eine typische lamellare flüssigkristalline Phase entwickelt nach längerer Lagerung unter polarisiertem Licht dunkle pseudoisotrope Bereiche. Diese Bereiche sind klar von den stark doppelbrechenden Bereichen getrennt. Die Lαh-Phase, die im mittleren Konzentrationsbereich der flüssigkristallinen Phase bei relativ hohen Temperaturen auftritt, zeigt solche Texturen. Schlierentexturen werden nie beobachtet, obwohl meist stark doppelbrechende ölige Schlieren vorhanden sind. Kühlt man eine Probe mit einer Lαh-Phase ab, um den Krafft-Punkt zu bestimmen, verändert sich die Textur unterhalb einer charakteristischen Temperatur. Die pseudoisotropen Bereiche und die klar definierten öligen Schlieren verschwinden. Zunächst kristallisiert kein C12-14-APG, sondern es bildet sich eine neue lyotrope Phase mit nur schwacher Doppelbrechung. Bei relativ hohen Konzentrationen dehnt sich diese Phase bis zu hohen Temperaturen aus. Bei Alkylglykosiden zeigt sich eine andere Situation. Alle Elektrolyte, mit Ausnahme von Natriumhydroxid, führten zu einer signifikanten Absenkung der Trübungspunkte. Der Konzentrationsbereich der Elektrolyte liegt etwa eine Größenordnung unter dem der Alkylpolyethylenglykolether. Überraschenderweise gibt es nur sehr geringe Unterschiede zwischen den einzelnen Elektrolyten. Durch Zugabe von Lauge wurde die Trübung deutlich reduziert. Zur Erklärung der Verhaltensunterschiede zwischen Alkylpolyglykolethern und Alkylpolyglykolethern wird angenommen, dass die in der Glucoseeinheit angereicherte OH-Gruppe unterschiedliche Arten der Hydratisierung mit der Ethylenoxidgruppe durchlaufen hat. Der deutlich stärkere Einfluss der Elektrolyte auf die Alkylpolyglykolether lässt darauf schließen, dass sich auf der Oberfläche der Alkylpolyglycosid-Mizellen eine Ladung befindet, während die Alkylpolyethylenglykolether keine Ladung annehmen.
Alkylpolyglycoside verhalten sich daher wie Mischungen aus Alkylpolyglykolethern und anionischen Tensiden. Die Untersuchung der Wechselwirkung zwischen Alkylglycosiden und anionischen bzw. kationischen Tensiden sowie die Bestimmung des Potentials in der Emulsion zeigen, dass die Alkylglycosid-Mizellen im pH-Bereich von 3 bis 9 eine negative Oberflächenladung aufweisen. Im Gegensatz dazu ist die Ladung von Alkylpolyethylenglykolether-Mizellen schwach positiv oder nahe Null. Der Grund für die negative Ladung von Alkylglycosid-Mizellen ist noch nicht vollständig geklärt.
Veröffentlichungszeit: 22. Oktober 2020





